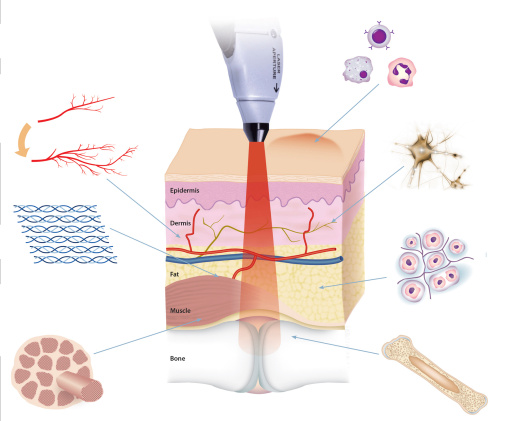
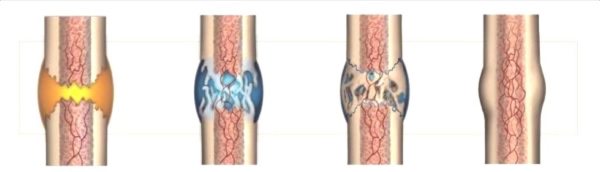
Από την έναρξη της ζωής στη γη, το φως υπήρξε μια από τις θεμελιώδεις πηγές βιολογικής ενέργειας.
Τα τελευταία χρόνια ανακαλύπτουμε πως μια ιδιαίτερη μορφή φωτός – το LASER, φως δηλαδή μόνο μίας συχνότητας/χρώματος – μπορεί να αποτελέσει κλειδί για την θεραπεία δεκάδων πολύ διαφορετικών διαταραχών.
Η θεραπεία με λέιζερ χαμηλής ισχύος (LLLT) είναι μία ιατρική μέθοδος κατά την οποία ανθρώπινος ιστός ακτινοβολείται με φως από ένα λέιζερ ιδιαίτερα χαμηλής ισχύος (της τάξης των μερικών εκατοντάδων μιλιβάτ) με σκοπό να προκαλέσει θεραπευτικά αποτελέσματα. Η μέθοδος αυτή χρησιμοποιείται εδώ και αρκετά χρόνια στην κλινική πράξη επιδεικνύοντας σταθερά το υψηλό θεραπευτικό δυναμικό της, αλλά μέχρι στιγμής δεν ήταν ξεκάθαρες οι βιοχημικές διεργασίες που οδηγούν το θεραπευτικό αυτό δυναμικό της. Το 2017 μια καινούργια μελέτη από δύο ιάπωνες επιστήμονες (Biological Function of Low Reactive Level Laser Therapy (LLLT), By Toshihiro Kushibiki and Miya Ishihara) έριξε φως σε αυτές ακριβώς τις κυτταρικές, μοριακές και βιοχημικές διεργασίες.
Η Ιστορία των θεραπευτικών LASER, ξεκινά «επίσημα» το 1968 όταν ένας Γερμανός ερευνητής, ο Μέστερ, προσπάθησε να εξερευνήσει το το καρκινογενετικό δυναμικό του φωτός λέιζερ, τη δυνατότητά του δηλαδή να προκαλεί καρκίνο! Στην έρευνά του αυτή ο Μέστερ, ακτινοβόλησε με φως λέιζερ χαμηλής ισχύος μία ξυρισμένη περιοχή του δέρματος κάποιων ποντικιών. Προς έκπληξή του και σε αντίθεση με τις προσδοκίες του, το φως από το λέιζερ όχι μόνο δεν προκάλεσε καρκίνο αλλά υποβοήθησε ισχυρά την ανάπτυξη των τριχών της περιοχής του δέρματος που είχαν ξυριστεί.
Από τότε έχουν αλλάξει πολλά. Αν και η μέθοδος εφαρμόζεται στην κλινική πράξη για πάνω από 50 χρόνια, και μεγάλος αριθμός από εργαστηριακές καθώς και κλινικές μελέτες δημοσιεύονται κάθε χρόνο στο πεδίο του LLLT, παρ’ όλα αυτά η συγκεκριμένη μέθοδος δεν έχει καταφέρει να λάβει την θέση που της αρμόζει στην πρώτη γραμμή της κλινικής πράξης. Ένας από τους λόγους είναι διότι οι παράμετροι ακτινοβόλησης διαφέρουν πολύ ανάμεσα στους χειριστές, κατασκευαστές και περιπτώσεις τέτοιων θεραπειών και θεραπευτές με μικρή γνώση ή πείρα στο συγκεκριμένο αντικείμενο δεν καταφέρουν να έχουν τα θεραπευτικά αποτελέσματα που θα μπορούσαν να επιτύχουν.
Η έρευνα του 2017 αποκάλυψε ότι αυτό ισχύει ακόμα και σε βιοχημικό επίπεδο αφού οι βιολογικοί μηχανισμοί στους οποίους βασίζονται τα θεραπευτικά αποτελέσματα διαφέρουν σημαντικά ανάλογα με τον τύπο του λέιζερ που χρησιμοποιείται, τον θεραπευτικό στόχο και άλλες πειραματικές συνθήκες.
Οι θεραπευτικοί στόχοι της μεθόδου είναι πολλοί και – περιέργως – αρκετά διαφορετικοί μεταξύ τους: Ξεκινώντας από τις δημοσιεύσεις του ίδιου του Μέστερ και των συνεργατών του για το θεραπευτικό δυναμικό του LASER στην επιτάχυνση της επούλωσης πληγών, πειραματικές και κλινικές μελέτες έδειξαν περεταίρω σημαντικές επιδράσεις της θεραπείας LLLT σε πολύ διαφορετικές διαταραχές, όπως:
- την αύξηση της σύνθεσης κολλαγόνου
- την αύξηση στον πολλαπλασιασμό κυττάρων χωρίς καρκινικό δυναμικό και μάλιστα ακόμα και κυττάρων που αναγεννώνται πολύ δύσκολα όπως αυτά του νευρικού ιστού!
- την επιτάχυνση στην πόρωση καταγμάτων
- τη τόνωση της κυκλοφορίας του αίματος
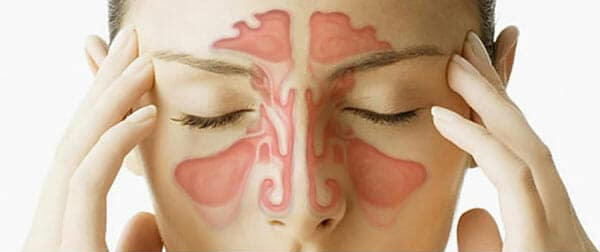
- τη καταστολή της φλεγμονής σε όλα τα επίπεδα, ακόμα και σε τόσο διαφορετικές αιτιολογίες όσο μια βακτηριακή λοίμωξη ή ένα πρήξιμο των ρινικών κογχών (βούλωμα της μύτης) λόγω αλλεργίας
- τη καταστολή του πόνου!
Φωτοβιολογία, φωτοϋποδοχείς και φωτοβιοτροποποίηση
Η μελέτη του 2016 ανήκει σε ένα καινούργιο επιστημονικό πεδίο, αυτό της φωτοβιολογίας που μελετά την επίδραση του φωτός σε βιολογικά συστήματα. Εισάγει δε καινούργιους επιστημονικούς όρους όπως «φωτοβιοτροποποίηση» (photobiomodulation) και ερευνά ειδικούς ενδοκυττάριους και εξωκυττάριους υποδοχείς φωτός που υπάρχουν σε όλα τα βιολογικά συστήματα.
Στη φωτοβιολογία, κεντρικό φαινόμενο είναι η φωτουποδοχή, δηλαδή μια ενδοκυττάρια διαδικασία κατά την οποία συγκεκριμένα βιομόρια που ονομάζονται φωτοϋποδοχείς και αντιδρούν σε ενέργεια συγκεκριμένου μήκους κύματος (όπως αυτό του λέιζερ), απορροφούν ενέργεια φωτονίων. Η μιτοχονδριακή αναπνευστική αλυσίδα είναι ένα κλασσικό παράδειγμα μιας πολύ κοινής βιοχημικής διεργασίας που περιλαμβάνει πολλούς φωτοϋποδοχείς. Οι τρεις από τους πιο σημαντικούς φωτοϋποδοχείς είναι η οξειδάση του κυτοχρώματος c, οι πορφυρίνες και οι φλαβοπρωτεϊνες.
Οξειδάση του κυτοχρώματος c: Η συγκεκριμένη οξειδάση έχει προταθεί ως ο κύριος ενδογενής φωτοϋποδοχέας για φως στο ορατό και εγγύς υπέρυθρο του φάσματος. Έχει μελετηθεί εκτενώς ειδικά για νευρικά κύτταρα. Πολλές μελέτες σχετικά με την ανάπτυξη των κυττάρων έχουν αναφέρει πως μετά από ακτινοβόληση παρατηρούνται αλλαγές στη δραστηριότητα της οξειδάσης και στην επακόλουθη παραγωγή ΑΤΡ, του κύριου βηλαδή ενεργειακού νομίσματος του οργανισμού .
Πορφυρίνες: Οι πορφυρίνες είναι μια ομάδα μακροκυκλικών οργανικών ενώσεων. Αυτές οι ενώσεις έχουν κυρίως πράσινο ή κόκκινο χρώμα, απορροφούν φως σε συγκεκριμένα μήκη κύματος χρώματος και εκπέμπουν ερυθρό φθορισμό. Οι φυσικώς απαντώμενες πορφυρίνες, συμπεριλαμβανομένων εκείνων που βρίσκονται στο ανθρώπινο σώμα, συχνά σχηματίζουν σύμπλοκα με ιόντα σιδήρου ή μαγνησίου. Όταν διεγείρονται με απορρόφηση φωτονίων λέιζερ, δημιουργούν ρίζες οξυγόνου που χρησιμοποιούνται από τον οργανισμό για αντιμετώπιση λοιμώξεων ή άλλων καταστάσεων βιολογικών εισβολέων. Με βάση τη γνώση αυτή έχει αναπτυχθεί ένας τρόπος φωτοδυναμικής θεραπείας για αντικαρκινική δράση.
Φλαβοπρωτεΐνες: Οι φλαβοπρωτεΐνες μεσολαβούν σε ένα ευρύ φάσμα βιολογικών διεργασιών, όπως βιοφωταύγεια, εξουδετέρωση ριζών οξυγόνου που προκαλούνται από οξειδωτικό στρες (ναι, αυτές που αναφέραμε πιο πάνω), επιδιόρθωση του DNA και απόπτωση (θάνατος) γηρασμένων κυττάρων. Ένας μεγάλος αριθμός ερευνητών, συμπεριλαμβανομένων και των συγγραφέων της μελέτης, έχουν αποκαλύψει σημαντικούς ρόλους των φλαβοπρωτεϊνών ως ενδοκυτταρικών φωτοϋποδοχέων. Απορροφούν φως κυρίως στα 350 – 500nm δηλαδή στο ορατό και εγγύς υπεριώδες τμήμα του φάσματος.
Εκτός από τις τρεις κύριες ομάδες φωτοϋποδοχέων που αναφέρθηκαν παραπάνω, υπάρχουν και άλλοι τύποι φωτοϋποδοχέων, συμπεριλαμβανομένων πολύ γνωστών ενώσεων όπως χολερυθρίνης, μελανίνης, βιταμίνης Β6, βιταμίνης Κ, NAD-P-H, και τρυπτοφάνης.
Πέρα από τις βιοχημικές αλλαγές που προκαλεί η θεραπεία LLLT με την απορρόφηση της φωτεινής ενέργειας από τους φωτοϋποδοχείς, οι ερευνητές συμφωνούν πως η ενέργεια των φωτονίων που συλλαμβάνεται από ενδοκυτταρικούς υποδοχείς οδηγεί και σε αλλαγές στην έκφραση γονιδίων και πρωτεϊνών.
Παραδείγματα αποτελούν οι μεταγραφικοί παράγοντες που μεσολαβούν σε πλήθος λειτουργιών των κυττάρων. Πολλές έρευνες καθιστούν σαφές ότι τα επίπεδα έκφρασης πολλών μεταγραφικών παραγόντων τροποποιούνται κατά την έκθεση τους σε ακτινοβολία λέιζερ. Έναν από τους σημαντικότερους μεταγραφικούς παράγοντες αποτελεί ο πυρηνικός παράγοντας NF -κB. Ως μεταγραφικός παράγοντας, ο ΝF-κΒ μπορεί ταυτόχρονα να επάγει την έκφραση ιντερλευκίνης IL-1, IL-2, IL-6, IL-8, IL-12, παράγοντα νέκρωσης όγκου TNF-α και άλλων προφλεγμονωδών κυτταροκινών. Ελέγχει επίσης την έκφραση των σχετιζόμενων με την απόπτωση πρωτεϊνών, οι οποίες παίζουν κρίσιμο ρόλο στην ανάπτυξη και την αθανασία των καρκινικών κυττάρων.
Τελευταίος, αλλά όχι και λιγότερο σημαντικός στις βιολογικές επιδράσεις του φωτός λέιζερ αποτελεί ο Κιρκάδιος ρυθμός: Ο κιρκάδιος ρυθμός, το εσωτερικό ρολόι του οργανισμού, είναι ένας κύκλος κυτταρικών συμβάντων διάρκειας 24 ωρών, που πιθανότατα αποκτήθηκε κατά τα πρώτα στάδια της εξέλιξης και είναι πανταχού παρόν, από μονοκύτταρους οργανισμούς μέχρι και στα θηλαστικά. Αρκετά γονίδια του κιρκάδιου αυτού ρολογιού των θηλαστικών συνεργάζονται για να δημιουργήσουν τη σταθερή επανάληψη των 24 ωρών. Ειδικές πρωτεΐνες του κιρκάδιου ρολογιού, όπως η πρωτεΐνη 2, η Clk και άλλες ορίζουν το ρυθμό του ρολογιού σε σχεδόν όλους τους τύπους κυττάρων (π.χ. ρυθμός κυτταρικής διαίρεσης). Η αναδιαμόρφωση των οστών είναι μια συνεχής τέτοια ομοιοστατική διαδικασία που περιλαμβάνει απορρόφηση υφιστάμενων οστών από οστεοκλάστες και σχηματισμό νέου οστού από οστεοβλάστες.
Πειράματα που διεξήχθησαν έδειξαν πως μετά από ακτινοβόληση με λέιζερ χαμηλής ισχύος αλλάζει το πρωτεϊνικό προφίλ των κιρκάδιων πρωτεϊνών με αποτέλεσμα την επιτάχυνση διαδικασιών όπως για παράδειγμα στην αποκατάσταση οστικών βλαβών.
Θεραπευτικές Επιδράσεις της ακτινοβόλησης με LASER
Σε κλινικό επίπεδο, όπως αναφέραμε και πιο πάνω, η ακτινοβόληση με λέιζερ χαμηλής ιχύος, μπορεί να επάγει θεραπευτικό αποτέλεσμα σε ένα μεγάλο εύρος διαταραχών.
Οι επιστήμονες μόλις πρόσφατα ξεκινούν να ξεδιαλύνουν τους βιολογικούς μηχανισμούς με τους οποίους συμβαίνει αυτό.
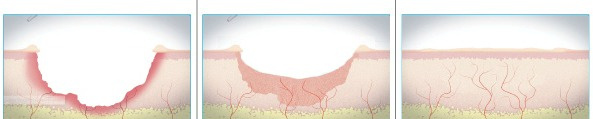
Για παράδειγμα ως προς τις βιολογικές επιδράσεις της θεραπείας LLLT στην επούλωση πληγών, μελέτες σε κύτταρα τα οποία ακτινοβολούνταν με λέιζερ, αποκάλυψαν πως η ακτινοβόληση προκαλούσε αύξηση των επιπέδων του αγγειακού ενδοθηλιακού αυξητικού παράγοντα (VEGF) καθώς και της έκφρασης του μετασχηματιστικού αυξητικού παράγοντα β (TGF β). Τα ευρήματα αυτά έδειξαν πως με τη χρήση λέιζερ σε κερατινοκύτταρα και ινοβλάστες, τους βασικούς δηλαδή κυτταρικούς μεσολαβητές της διαδικασίας επούλωσης τραύματος, ενισχύεται η έκφραση πολλών κυτταροκινών και αυξητικών παραγόντων με αποτέλεσμα να επιταχύνεται σημαντικά η διαδικασία της επούλωσης.
Ως προς την αντιφλεγμονώδη δράση της θεραπείας LLLT, πειράματα που διεξήχθησαν έδειξαν πως η ακτινοβόληση με λέιζερ καταστέλει την παραγωγή φλεγμονωδών κυτοκινών και τη μετανάστευση φλεγμονωδών κυττάρων.
Επίσης η ακτινοβόληση με χαμηλής ισχύος λέιζερ επιδρά θεραπευτικά στον αρθρικό χόνδρο και στον μυϊκό ιστό ενώ την ίδια στιγμή βοηθάει στην αναγέννηση των κατεστραμμένων νευρώνων και τη μείωση του πόνου.
Τέλος, η θεραπεία LLLT παρέχει και αισθητικά οφέλη συντελώντας στην ανάπτυξη και αναγέννηση των μαλλιών, στην θεραπεία της ακμής και στην αναζωογόνηση του δέρματος.
Η τεχνολογία των LASER χαμηλής ισχύος αποτελεί μια εξαιρετική επιλογή για θεραπεία μιας πλειάδας διαταραχών από πόρωση καταγμάτων ως αποσυμφόρηση της μύτης!
Καλέστε μας τώρα στο 2311 82 11 00 για πληροφορίες!